| 元素 | Al | Zn | Mn | Si | Fe | Cu | Mg |
|---|---|---|---|---|---|---|---|
| 质量分数/% | 2.3~3.5 | 0.5~1.5 | 0.15~0.5 | <0.25 | <0.05 | <0.05 | 余量 |
分享:Li2CrO4缓蚀剂对镁电池负极耐蚀性及电化学性能的改善
随着世界各国对能源需求量的与日俱增[1],能源革新迫在眉睫。锂离子电池虽然能缓解能源消耗,但锂电池安全性差、锂矿资源少[2]等缺点注定了其只能成为能源的过渡形式。在金属电池体系中,镁电池无污染、能量高、体积小、质量轻、安全性高、价格低廉[3],是一种极具前景的储能设备。镁与锂处于元素周期表的对角线位置上,因此具有很多相似的化学性质[4]。理论上,镁电池可发展的空间远超过锂电池,镁的标准电极电位在-2.36 V (相对于标准氢电极),可以组成较大的开路电压和工作电压,且由于镁的电化学当量小[0.454 g/(A·h)][5],其理论比容量可高达2 205 mA·h/g[6]。因此,镁电池成为了储备电池首选,尤其是水系镁锰电池,已经在日本实现商用化。但金属镁比较活泼,在水系电解液中容易腐蚀。纯镁的腐蚀速率过大、阳极利用率低以及阳极极化严重等原因使得其难以满足电池负极材料的使用要求。用AZ31镁合金代替纯镁作为镁电池负极[7]能够降低自腐蚀速率,提高利用率。此外,在放电过程中,镁电池电压滞后明显[8],这与镁电池在水系电解液中的副反应有关。通常在电解质溶液中,镁极易生成Mg(OH)2[9]或者MgO并在电极表面积累生成钝化膜[10],阻滞负极反应,同时影响放电的进行。因此,电解液对镁电池体系的影响巨大,寻找适宜的电解液添加剂对镁电池发展具有重要意义。科研人员希望通过添加缓蚀剂[11]减缓放电过程中钝化膜的形成[12],以缩短镁电池的电压滞后时间,改善水系镁电池放电性能[13]。铬酸锂(Li2CrO4)作为电解液缓蚀剂能够改善镁电池中阳极极化,减小自腐蚀速率[14],降低过电位和自腐蚀性。作者以AZ31镁合金作为负极材料,在Mg(ClO4)2电解质溶液中添加不同量Li2CrO4缓蚀剂,研究了Li2CrO4的缓蚀效果和电化学性能,并组装了水系镁锰电池,采用恒流放电测试仪研究电池的放电行为。
1. 试验
试验材料为AZ31挤压态镁合金薄片,其化学成分如表1所示,显微组织见图1。对比铸态和挤压态AZ31镁合金组织,可以看出镁合金在挤压过程中形成了大小均匀的动态再结晶晶粒。试验介质为0.72 mol/L Mg(ClO4)2溶液,向其中添加缓蚀剂Li2CrO4,缓蚀剂的质量分数分别为0、0.3%、0.7%、1.0%、1.2%。
将AZ31镁合金试样置于添加不同量Li2CrO4的Mg(ClO4)2溶液中进行浸泡腐蚀试验,浸泡时间为168 h。采用失重法计算镁合金试样的腐蚀速率,再根据腐蚀速率计算缓蚀剂的缓蚀率。
将试验材料加工成20 mm×20 mm×5 mm的电极试样。试样经120号~1000号砂纸依次打磨,然后用酒精和丙酮清洗并吹干备用,使用时先连接电极引线,再用环氧树脂镶嵌绝缘。电化学试验采用三电极体系:工作电极为AZ31镁合金(工作面积1 cm2);辅助电极为铂电极;参比电极为饱和甘汞电极(SCE)。电化学测试由AUTOLAB PGSTAT302N型电化学工作站完成。
对水系镁锰电池进行组装。电解液采用0.72 mol/L的Mg(ClO4)2溶液,并添加了不同量Li2CrO4缓蚀剂;负极采用厚度为0.5 mm的AZ31镁合金板,面积为10 cm2;正极采用88%(质量分数,下同)MnO2、9%乙炔黑和3%羟甲基纤维素钠的复合材料(将按比例配制的三种材料置于球磨罐中球磨8 h,涂于泡沫镍上并烘干)。正负极上各嵌上密封垫圈,并且正负极上部都有注液孔,用于注入电解液。中间是亲水性的PE电池隔膜。通常,将制作好的电池于常温室中静置5 min,待电解液与正负极充分接触后再进行放电测试。电池放电数据由LAND CT2001A型恒流放电测试仪测得。测试温度保持在25 ℃,放电电流密度为1 mA/cm2,当电压低于0.6 V时放电结束。图2为组装电池恒流测试示意图。
放电结束后,采用JEOL JSM-6390LV型场发射扫描电镜(SEM)和Rigaku D/max 2200vpc型X射线衍射仪(XRD)对电极表面进行分析。
2. 结果与讨论
2.1 Li2CrO4用量对AZ31镁合金腐蚀行为的影响
由图3可以看出,随着缓蚀剂Li2CrO4用量的增加,AZ31镁合金在0.72 mol/L Mg(ClO4)2溶液中的腐蚀速率先减小后增大,而Li2CrO4的缓蚀率先增大后减小。当Li2CrO4质量分数为1.0%时,AZ31镁合金的腐蚀速率最小且Li2CrO4的缓蚀率最大。其原因可能是:当Li2CrO4质量分数不足0.3%时,Li2CrO4在AZ31镁合金表面形成的保护膜不完整,腐蚀性 在未成膜区的吸附加强,并诱发了点蚀,Li2CrO4的缓蚀率不高;当Li2CrO4质量分数达1.0%时,Li2CrO4在AZ31镁合金表面形成完整致密的保护膜,缓蚀率达到最大;当Li2CrO4质量分数大于1.0%时,在AZ31镁合金表面形成的缓蚀剂保护膜开始溶解,缓蚀率下降,这将有利于离子传输。
在未成膜区的吸附加强,并诱发了点蚀,Li2CrO4的缓蚀率不高;当Li2CrO4质量分数达1.0%时,Li2CrO4在AZ31镁合金表面形成完整致密的保护膜,缓蚀率达到最大;当Li2CrO4质量分数大于1.0%时,在AZ31镁合金表面形成的缓蚀剂保护膜开始溶解,缓蚀率下降,这将有利于离子传输。
2.2 Li2CrO4用量对AZ31镁合金电化学行为的影响
2.2.1 极化曲线(Tafel)
图4为AZ31镁合金在添加不同量Li2CrO4的Mg(ClO4)2溶液中的极化曲线,对极化曲线拟合得到的电化学参数见表2。
| Li2CrO4质量分数/% | 自腐蚀电位(vs. SCE)/V | 钝化电位φ/V | 腐蚀电流密度/(μA·cm-2) | 极化电阻/(Ω·cm2) |
|---|---|---|---|---|
| 0 | -1.39 | - | 2.75 | 1 944 |
| 0.3 | -1.28 | -1.28~-1.23 | 0.36 | 22 523 |
| 0.7 | -1.27 | -1.27~-1.22 | 1.80 | 26 376 |
| 1.0 | -1.24 | -1.24~-1.12 | 0.10 | 55 910 |
| 1.2 | -1.26 | -1.26~-1.24 | 0.17 | 38 400 |
结果表明,在Mg(ClO4)2溶液中添加缓蚀剂Li2CrO4后,AZ31镁合金的自腐蚀电位出现正移,Li2CrO4质量分数为1.0%时,自腐蚀电位正移量最大,为150 mV,镁合金的腐蚀电流密度明显减小,极化电阻也显著增大。添加Li2CrO4后,阳极界面能增加,阳极氧化区出现了明显的钝化现象,这说明Li2CrO4属于阳极钝化型缓蚀剂,钝化区随着缓蚀剂用量增加而增大,Li2CrO4的添加显著提高了AZ31镁合金的电化学稳定性能。添加Li2CrO4后极化电阻显著增大,说明Li2CrO4在AZ31镁合金表面形成的钝化膜完整致密,阻止了腐蚀介质与其接触,从而起到良好的缓蚀作用。当Li2CrO4质量分数大于1.0%后,自腐蚀电位又稍微负移,腐蚀电流密度有所增大,钝化区减小,这说明添加过多的Li2CrO4不仅不能起到钝化保护作用,反而促进膜的溶解,这一现象说明Li2CrO4具有用量极值。当Li2CrO4的用量不足或超过一定的范围时,钝化膜不完整,会加速金属在溶液中的腐蚀。
2.2.2 电化学阻抗谱
由图5可知,在添加不同量Li2CrO4的0.72 mol/L Mg(ClO4)2溶液中,AZ31镁合金的电化学阻抗谱形状类似,均表现为一个近似半圆的中高频容抗弧,只是弧的直径不同,阻抗谱低频区均不存在由扩散引起的warburg阻抗,仅有一个时间常数。阻抗谱高频区容抗弧是由于电荷传递引起的,其直径可以近似看作电极反应的电荷传递电阻,阻抗谱高频区形成双电层电容,随着Li2CrO4用量的增加,圆弧半径先增大后减小,相应的电荷传递电阻也先增大后减小,缓蚀效果明显。Li2CrO4质量分数从0.3%增加到0.7%时,电荷传递电阻由1.9 kΩ·cm2逐渐增加到22 kΩ·cm2;当Li2CrO4质量分数为1.0%时,电荷传递电阻达最大,为45 kΩ·cm2,此时缓蚀效果最好。这表明随Li2CrO4用量的增加,AZ31镁合金表面形成的钝化膜层逐渐完整致密,溶液中的侵蚀性离子通过膜层的阻力增大。继续增加Li2CrO4用量,电荷传递电阻减小,缓蚀效果变差,这可能与钝化膜溶解有关。电化学阻抗谱表现出的规律与极化曲线基本吻合。
2.3 Li2CrO4用量对AZ31镁合金电池放电性能的影响
在添加不同量Li2CrO4缓蚀剂的0.72 mol/L Mg(ClO4)2溶液中AZ31镁合金电池的恒流放电曲线如图6所示,表3为对应的放电数据。结果表明,Li2CrO4缓蚀剂的加入不仅提高了AZ31镁合金电池的放电平台,并且有效增加了电池放电容量;当Li2CrO4质量分数为1.2%时,电池放电容量达196.9 mA·h,与不添加Li2CrO4的Mg(ClO4)2溶液相比,放电容量提高了约64%,放电中值电压在1.4 V左右,放电平台平滑、稳定。
| Li2CrO4质量分数/% | 恒流放电时间/h | 放电中值电压/V | 放电容量/(mA·h) |
|---|---|---|---|
| 0.0 | 12.0 | 1.39 | 120.0 |
| 0.3 | 12.8 | 1.42 | 128.3 |
| 0.7 | 17.0 | 1.45 | 171.0 |
| 1.0 | 15.3 | 1.32 | 152.7 |
| 1.2 | 19.6 | 1.39 | 196.9 |
由图7中可以看出:在不添加Li2CrO4的Mg(ClO4)2溶液中放电后,AZ31镁合金表面腐蚀膜疏松多孔,表面凹凸不平,从其截面图能看出明显的局部腐蚀;在添加Li2CrO4的Mg(ClO4)2溶液中放电后,AZ31镁合金表面很平整,从其截面图可见明显三层膜结构,内层较厚,中间层也较厚,但已经脱水龟裂,最外层比较致密,AZ31镁合金基体没有大的腐蚀坑,趋于全面腐蚀。
从图8所示XRD谱可以看出:在未添加Li2CrO4的Mg(ClO4)2溶液中放电后,AZ31镁合金表面物相为单一的Mg(OH)2相,添加Li2CrO4后物相变得多元化,增加了CrO[7,15]、Cr2O3、MgO等新的物相,并且Mg(OH)2峰强变弱。由此可以推测,Li2CrO4的加入抑制了镁合金的腐蚀反应。其反应机理可能是,当镁合金负极放电时,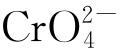 优先吸附于镁合金负极表面并通过自身氧化性先与镁合金负极反应,使镁合金负极表面形成MgO氧化层,而其自身被还原为Cr2+并在负极表面形成吸附膜,氧化层和吸附膜层能有效隔离镁合金基体与电解质接触,进而阻止腐蚀的发生[16]。因此,当Li2CrO4用量较少时(0.3%)其对电池的影响不大,放电容量提高甚微,当Li2CrO4质量分数超过0.3%时,电池放电容量有较大提高,当Li2CrO4质量分数为1.2%时,电池放电容量达最大。
优先吸附于镁合金负极表面并通过自身氧化性先与镁合金负极反应,使镁合金负极表面形成MgO氧化层,而其自身被还原为Cr2+并在负极表面形成吸附膜,氧化层和吸附膜层能有效隔离镁合金基体与电解质接触,进而阻止腐蚀的发生[16]。因此,当Li2CrO4用量较少时(0.3%)其对电池的影响不大,放电容量提高甚微,当Li2CrO4质量分数超过0.3%时,电池放电容量有较大提高,当Li2CrO4质量分数为1.2%时,电池放电容量达最大。
3. 结论
通过研究AZ31镁合金在添加Li2CrO4的Mg(ClO4)2电解液中的腐蚀行为了解电池中镁合金负极材料的腐蚀情况,并组装成水系镁锰电池探究其放电性能,得到如下结论。
(1)在Mg(ClO4)2电解液中添加Li2CrO4后,AZ31镁合金的耐蚀性得到提升。当Li2CrO4质量分数为0.7%时,溶液能够满足放电与耐蚀的要求。此外,随着Li2CrO4用量的升高,AZ31镁合金的自腐蚀电位明显正移,当Li2CrO4质量分数为1.0%时,自腐蚀电位正移量最大,达150 mV,腐蚀电流密度先降低后增大,因此耐蚀性先增强后减弱。
(2)Li2CrO4可以提高水系镁锰电池放电平台及放电容量。当Mg(ClO4)2电解液中Li2CrO4质量分数为0.7%时,放电平台提高0.15 V左右,当Li2CrO4质量分数为1.2%时,水系镁锰电池放电容量最大,为196.9 mA·h,相对空白溶液,电池的放电容量提高约64%。
(3)Li2CrO4的缓蚀机理主要与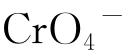 吸附膜有关,镁基体与
吸附膜有关,镁基体与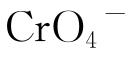 反应形成的钝化层能隔离镁负极与电解液接触,使腐蚀速率下降。
反应形成的钝化层能隔离镁负极与电解液接触,使腐蚀速率下降。
由此看来,含Li2CrO4电解液体系能够有效提升水系镁锰电池性能,对镁电池发展具有重要意义。目前,水系镁电池电解液体系中仍存在电解液成本高、随外界影响大等缺点。但在应急领域,水系镁电池的商用前景广阔。因此在接下来的工作中,应寻找应急领域的溶剂体系、降低应用成本,进一步推动镁锰电池向商用化发展。
文章来源——材料与测试网














 浙公网安备 33042402000106号
浙公网安备 33042402000106号

